Fascinující vhled do světa banality fascinujících biotechnologických postupů
Vzhledem k tomu, že ve světě se dějí strašlivé věci, rozhodl jsem se udělat malé ublognutí na wholesome téma. Určitě jste už slyšeli o genové editaci pomocí CRISPR-Cas9, možná nevíte co přesně dělá, a hlavně jak přesně se to, z praktického pohledu na věc, tzn. rukama, dělá.
Odpustím si wikipedistický úvod a napíšu to spíše z hlavy: podobně jako dávno známé restrikční endonukleázy (enzymy, které štěpí specifickou, zpravidla palindromatickou, sekvenci v nukleové kyselině), je CRISPR-Cas9 technologie založená na jakémsi fyziologickém obranném mechanismu existujícím v určitém druhu bakterie. Cas9 je vlastně další endonukleáza, narozdíl od těch běžných ale pracuje ve spojení s guide RNA molekulou. V oblasti s odpovídající sekvencí, se kterou se guide RNA spáruje, pak Cas9 vytvoří double strand break, tedy přestřihne v daném místě obě vlákna dvoušroubovice
To je nesmírně cenná možnost, protože před vynálezem CRISPR-Cas9 (a jejího méně osvědčeného předchůdce, zinc finger nukleáz) nebylo vytváření takto precizních zlomů v zásadě možné – zpravidla jsme při genovém inženýrství museli spoléhat na náhodně se vyskytující štěpná místa pro restrikční endonukleázy. K čemu je to ale dobré?
V zásadě tím lze dosáhnout dvou možných cílů – knock in a knock out mutací. Při knock in se do specificky dosaženého zlomu něco vkládá, a s tím zkušenosti nemám a proto to nebudu popisovat. Při vytváření knock outu se zpravidla využívá mechanismu non-homologous end joining. Není nutno do vysvětlování tohoto mechanismu příliš zabředávat, ale je až legrační, v čem spočívá princip jeho využití.
Pokud se vytvoří zlom, buňka se pokusí pomocí mechanismu non-homologous end joining zlom opravit. Velmi často to udělá úspěšně, ale v části případů se splete o zpravidla jeden nukleotid (tedy písmeno v sekvenci) – buď jeden vynechá, nebo jeden vloží. Vzhledem k tomu, že genetický kód je zapsaný v tripletech, tedy trojicích písmen, tohle má za následek, že přidáním či smazáním jednoho písmena dojde k posunu čtecího rámce, a to má zase za následek, že od daného místa v sekvenci je kódovaný protein (o jehož knock-out, tedy vyřazení z provozu, nám zpravidla jde) čten nesprávně, ale nejen to, nevyhnutelně pak translační mašinerie naráží na výskyt stop kodónu v tomto jiném čtecím rámci. Místo cíleného proteinu tedy vzniká jeho nedokončená verze, kterou buňka rozpozná jako něco, čeho je se potřeba zbavit.
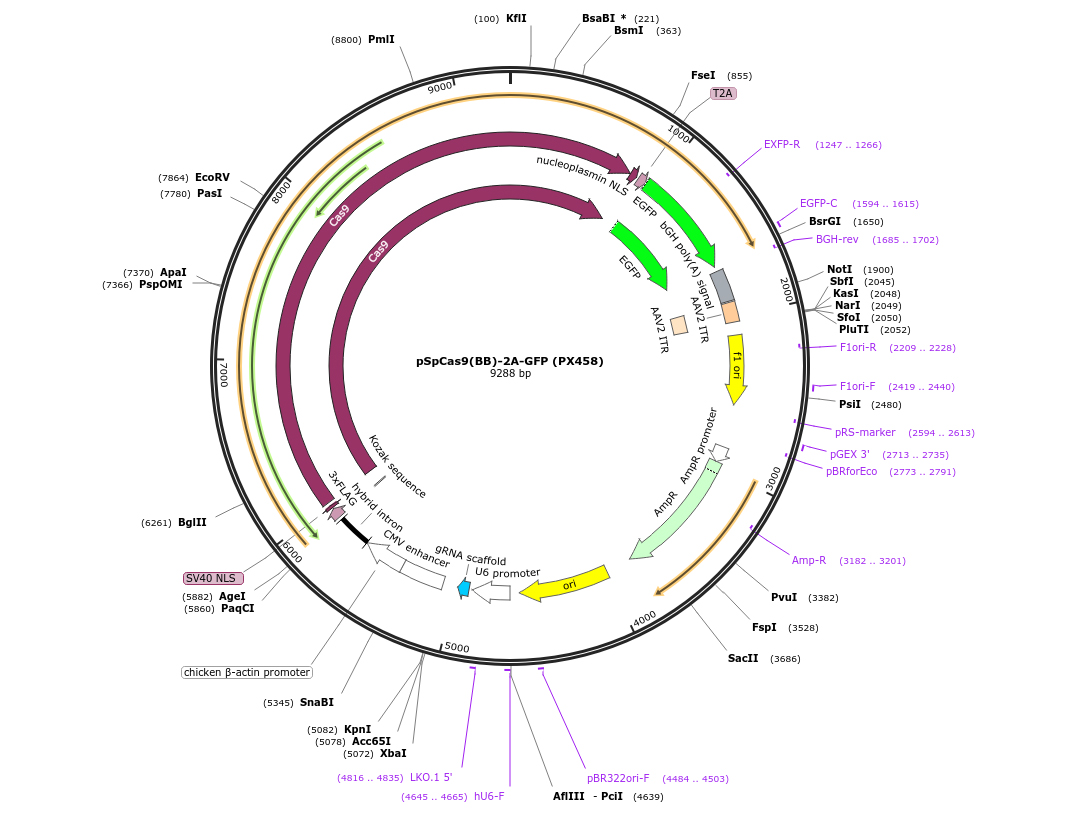
Pokud si chcete navrhnout svůj CRISPR-Cas9 systém, jsou na to dnes samozřejmě user friendly algoritmické webové aplikace, kam zadáte cílový gen a alogritmus vám předloží statisticky nevhodnější zásahová místa. Na jejich základě si objednáte krátký oligonukleotid, který pomocí starých dobrých molekulárně biologických metod vložíte to rovněž user-friendly plasmidu, který vám pomocí starých dobrých molekulárně biologických metod namnoží vaše kamarádky E. coli.
Plasmid pak pomocí osvědčených metod transfekujete do buněk, kde se z něj jednak přepíše guide RNA a jednak také Cas9 endonukleáza, která provede svou činnost. Buňky můžete nějak selektovat, například pomocí antibiotika, já ale použil jiný high-tech mechanismus: plasmid nese rovněž zelený fluorescenční protein z medúzky, díky kterému po transfekci buňky pár dní svítí. Tou dobou se pak dají vysortovat průtokovým cytometrem. Naše facilita nabízí možnost vysortovat jednotlivé svítící buňky do jamek v 96jamkových destičkách. Ty pak po nějakém čase a při troše štěstí a vlídném zacházení narostou do klonů. Klony pak můžete nechat v cílové oblasti genomu osekvenovat a ověřit, zdali a k jaké mutaci došlo.