Je to můj web, takže můžu v osvětových postech používat v nadpisech invektivy
Jeden ze vzorců, který se v živých systémech často opakuje, je leckdy překvapivě odlišné působení léčiv a přírodních látek při dramatickém rozdílu jejich koncentrací vnesených do živých systémů. Příkladem může být prachsprostý kofein, který známe jako životabudič schopný působit na neurotransmitery, ale v o několik řádů vyšší koncentraci může působit na buněčný cyklus, čehož se využívá při synchronizaci buněk in vitro. Nebo například metformin, antidiabetické léčivo, které působením na AMP dependentní kinázu snižuje hladiny glukózy v krvi, ale při výrazně vyšších koncentracích působí na mTOR a vykazuje antiproliferační účinky využitelné proti rakovinným buňkám.
Dalším takovým příkladem, jemuž se v tomto terapeutickém ublognutí chci věnovat, je látka jménem sertralin, mnohým lépe známá pod obchodním názvem Zoloft. Při běžných dávkách okolo 50-200 mg/den je nejtypičtěji užíván jako antidepresivum, zvýšíme-li tuto dávku na cca 50x, setralin vykazuje antiproliferační účinky. Mechanismus účinku setralinu coby antidepresiva je dobře známý, funguje jako jeden z mnoha inhibitorů zpětného vychytávání serotoninu v nervových synapsích mozku. Konkrétně působí na serotoninový transportér SERT/SLC6A4 a brání vychytávání 5-hydroxytryptaminu. Mechanismus účinku jako cytostatika je trochu problematičtější vysvětlit, protože dosahuje zcela nevšední úrovně pleiotropismu (to je takové chytře znějící slovo které znamená “dělá to hodně různých věcí”).
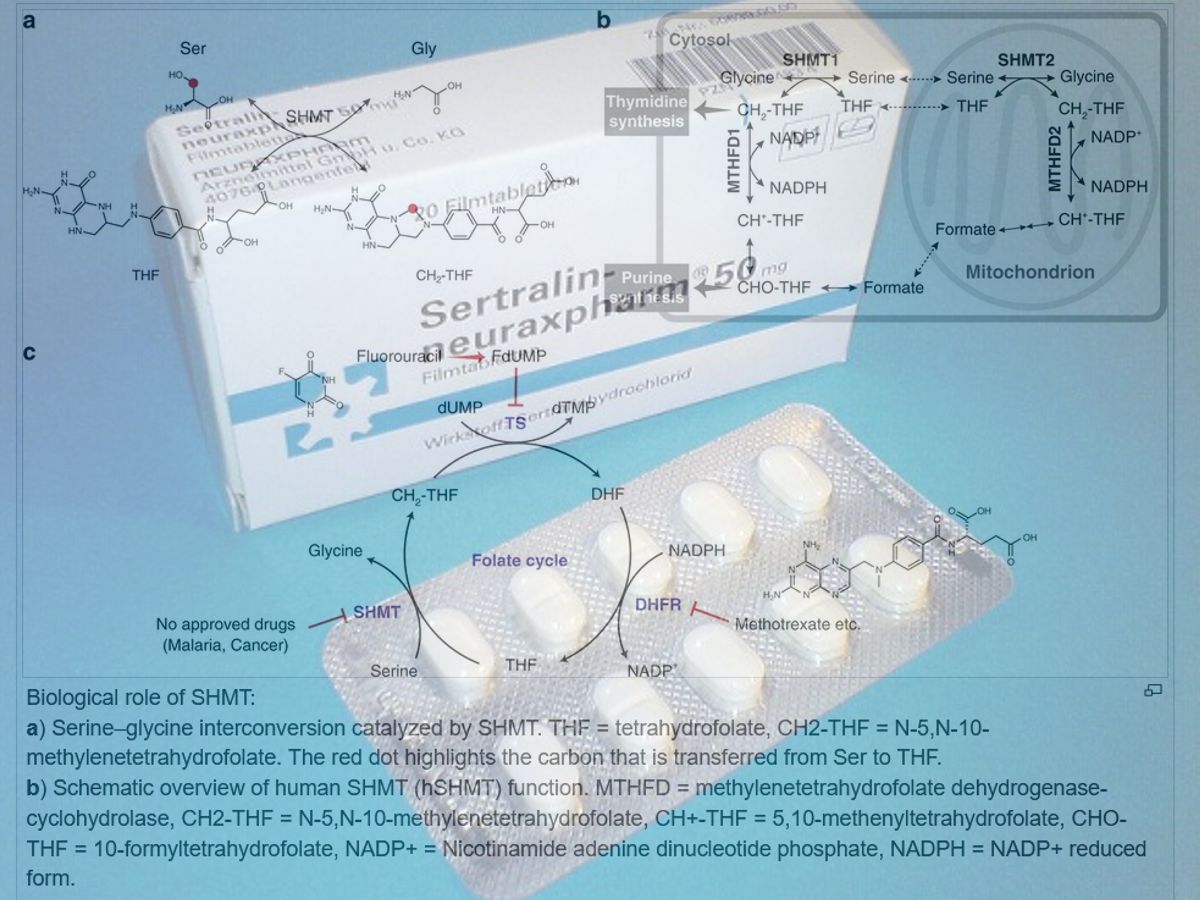
Z pleiotropické škály cytostatických účinků poněkud vybočuje inhibice enzymů SHMT1 a SHMT2, což jsou serin hydroxymethyltransferázy, jedna se nachází v cytoplazmě, druhá v mitochondriích, a katalyzují tutéž reakci - jak naznačuje název: transfer hydroxymethylu ze serinu za vzniku glycinu (a taky naopak, reakce je reverzibilní). Není to ale jen otázka konverze aminokyselin. Tato reakce je bezprostředně spojená s folátovým cyklem (cyklem kyseliny listové). Při něm díky SHMT1/2 vzniká z tetrahydrofolátu methylentetrahydrofolát, a ten je zase potřeba pro thymidylát syntázu. Thymidylát začíná na T a to je jedno ze čtyř písmenek v genetickém kódu DNA. Skutečně se jedná přesně o tohle konkrétní T, a tento enzym je tedy potřeba i k tomu, aby se DNA mohla kopírovat a to je zas potřeba k tomu, aby se buňky mohly dělit a to je samotná podstata nejen života, ale taky rakoviny. A zatímco rakovinu chcete zabít, občas musíte člověka trochu přizabít, třeba inhibicí nějaké klíčové metabolické dráhy. Ano, třeba jako sertralin, který působí hned na dvě o kterých jsem psal o pár řádek výš, folátový cyklus a na něj navázanou syntézu DNA, a metabolismus aminokyselin a na něm závislou syntézu proteinů.
Dalšími mechanismy, které se v literatuře objevují a doplňují tak pleiotropický bestiář, jsou poněkud hůře uchopitelné. Suprese prorůstové dráhy mTOR, stres endoplazmatického retikula, překonání rezistence k apoptóze, působení přes regulační protein TCTP… Řekněme, že nedávné review vyvolává dojem, že skrumáž těchto mechanismů a snaha rámovat ji jako multimodalitu sertralinu je možná lehce na vodě, zatímco působení na SHMT1/2 je vcelku jasně prokázané na buňkách závislých na syntéze serinu a glycinu.
V tomto mechanismu se možná skrývá klíč k využití sertralinu v onkologii - nikoli jako univerzální cytostatikum (a nebuďme v prezentaci nadějných látek v odborné literatuře neskromní až nestoudní), ale jako selektivní zbraň proti nádorům s určitým metabolickým profilem. Otázkou samozřejmě zůstává, jak dosáhnout potřebných koncentrací bez toxicity - ale to je již výzva pro farmakology a chemiky. Já jen vraždím myši a zalívám buňky Savem.